MODUL IPA
PETUNJUK BELAJAR:
Langkah-langkah yang harus kalian lakukan dalam PJJ dengan menggunakan MODEL DABLOG ini adalah sebagai berikut.
1. Usahakan memiliki buku siswa cetakan terbaru (dari perpustakaan sekolah)
2. Baca dan pahamilah tujuan pembelajaran dengan baik.
3. Selesaikan Bab ini dalam 3 x pertemuan dengan rincian pertemuan pertama "Partikel penyusun benda dan Lambang Atom", dan pertemuan kedua " Konfigurasi Elektron dan Ikatan Kimia" dan "Praktik menyelidiki sifat bahan"
4. Mulailah mempelajari modul ini dengan fokus dan konsentrasi jangan lupa berdo'a, bila mengalami kesulitan diskusikan dengan temanmu atau gurumu.
5. Setelah kamu merasa memahami materi, kerjakan tugas dan latihan soal dalam buku tulismu.
6. Periksalah hasil pekerjaanmu dengan mencocokkan kunci jawaban dalam MODEL DABLOG ini.
7. Selanjutnya kerjakan tes akhir, bila kamu mendapatkan nilai sekurang-kurangnya 75 berarti kamu bisa melanjutkan ke KD berikutnya, jika belum kalian harus mengulang untuk mempelajari KD ini kembali.
A. PENDAHULUAN
Setiap benda memiliki karakteristik yang khas. Karakteristik yang dimaksud adalah sifat fisika dan sifat kimia benda. Bagaimana itu bisa terjadi, dan apa penyebabnya? Setelah kalian menyelesaikan modul ini, kalian akan menemukan jawabannya.
KOMPETENSI DASAR PENGETAHUAN :
3.8 Menghubungkan konsep partikel materi (atom, ion,molekul), struktur zat sederhana dengan sifat bahan yang digunakan dalam kehidupan sehari- hari, serta dampak penggunaannya terhadap kesehatan manusia
KOMPETENSI DASAR KETERAMPILAN:
4.8 Menyajikan hasil penyelidikan tentang sifat dan pemanfaatan bahan dalam kehidupan sehari-hari
Tujuan Pembelajaran:
1. Melalui PJJ siswa dapat menjelaskan penyebab benda memiliki sifat yang berbeda
2. Melalui PJJ siswa dapat mendeskripsikan atom penyusun benda
3. Melalui PJJ siswa dapat memahami lambang atom
4. Melalui PJJ siswa dapat menunjukkan rasa tanggung jawab, rasa ingin tahu dan disiplin.
B. KEGIATAN BELAJAR
Kegiatan Belajar 1
Materi dalam bentuk Audio-Visual ada di link berikut.
https://www.youtube.com/watch?v=QtKJ0u5QU2M&t=35s
A.
Partikel dalam
Benda dan Makhluk Hidup
Benda mati maupun makhluk hidup tersusun dari
partikel-partikel penyusunnya. Partikel tersebut dapat berupa atom-atom dan ion
yang saling berikatan satu sama lain membentuk molekul unsur dan molekul
senyawa. Senyawa-senyawa tersebut dapat berupa protein, karbohidrat, lemak, dan
lain sebagainya. Protein tersusun dari atom C, H, O dan N. Karbohidrat dan
lemak tersusun dari atom C, H, dan O.
Sifat fisika dan kimia setiap benda ditentukan
oleh jenis atom-atom penyusunnya, jumlah atom-atom penyusunnya, dan jenis
ikatan antar atom-atom penyusunnya. Contohnya adalah kayu dan ubi kentang.
Meskipun kayu dan ubi kentang tersusun dari jumlah dan jenis atom yang sama,
tetapi keduanya memiliki karakter yang berbeda. Hal ini disebabkan ikatan antar
atom yang terbentuk pada ubi dan kayu berbeda. Ubi memiliki sifat mudah dicerna
sehingga dapat dikonsumsi, sedangkan kayu memiliki sifat keras dan sulit
dicerna kecuali dibantu dengan enzim selulosa seperti yang dimiliki oleh rayap.
B.
Atom dan Partikel
Penyusunnya
1.
Partikel Subatom
Partikel terkecil penyusun benda disebut
dengan atom. Namun demikian atom-atom memiliki bagian yang yang lebih kecil
lagi yang disebut dengan partikel subatom. Perhatikan gambar model atom
berikut.
Inti atom terdiri dari proton dan neutron yang membentuk padatan karena diikat oleh energi ikat inti.
Kulit atom merupakan tempat beredarnya elektron yang senantiasa bergerak mengelilingi inti atom.
Banyaknya kulit atom tergantung dari banyaknya elektron.
Proton = partikel bermuatan positif
Elektron = partikel bermuatan negatif
Neutron = partikel tidak bermuatan
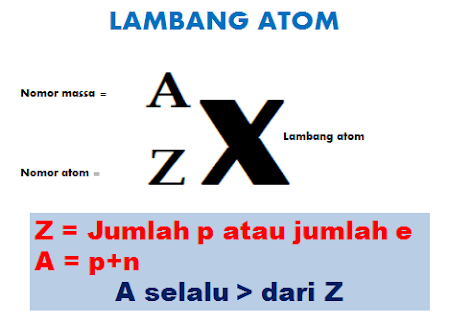
2. Nomor Atom dan Nomor Massa
Untuk memudahkan mempelajari atom dan
karakteristiknya, maka dibuatlah lambang atom yang unik sebagai berikut.
Nomor massa (A) merupakan angkan pembulatan yang selalu lebih besar dari nomor atom (Z).
Nomor atom menyatakan jumlah proton atau jumlah elektron.
Nomor massa menyatakan jumlah proton ditambah
jumlah neutron.
Perlu diketahui nomor massa menyatakan massa atom yang berasal dari proton dan neutron, sedangkan massa elektron diabaikan karena sangat ringan jika dibandingkan dengan proton dan neutron.
Nomor atom merupakan nomor urut susunan atom
pada SPU (Sistem Periodik Unsur) berupa baris (periode) dan kolom (Golongan).
TUGAS 1:
Jawablah
pertanyaan-pertanyaan berikut ini!
1.
Jelaskan mengapa,
setiap benda memiliki karakteristik yang khas sehingga berbeda dengan benda
lain?
2.
Deskripsikanlah
bagaimana bentuk dan komposisi sebuah atom!
3.
Perhatikanlah
gambar berikut!
Identifikasilah persamaan dan perbedaan antara gambar a dan gambar b!
4. Perhatikan gambar lambang atom berikut!
11Na23
a.
Lambang atom = …
b.
Nomor massa =
…
c.
Nomor atom = …
d.
Jumlah proton = …
e.
Jumlah elektron = …
f.
Jumlah neutron = …
Kegiatan Belajar 2
A.
Prinsip
Pembentukan Ion dan Molekul
1.
Konfigurasi
Elektron
Konfigurasi elektron merupakan susunan
elektron pada kulit-kulit atom. Untuk menyusun elektron pada kulitnya maka
harus memenuhi aturan aturan tertentu.
1. Kulit K harus terisi 2 atau kurang.
2. Kulit L maksimum terisi 8 atau kurang.
3. Untuk kulit ke M dan seterunya berlaku :
a) Jika sisa elektron lebih dari 8 dan kurang dari 18 maka harus diuraikan menjadi “8” dan sisanya lagi diisikan pada kulit berikutnya.
b) Lebih dari 18 dan kurang dari 32 maka harus diuraikan menjadi 18 dan sisanya selanjutnya mengikuti ketentuan nomor 1, tetapi kalau masih sama atau lebih dari 18 maka diuraikan lagi menjadi 18 dan sisanya selanjutnya mengikuti ketentuan no 1.
c) Lebih dari 32 maka harus diuraikan menjadi 32 dan sisanya selanjutnya mengikuti ketentuan nomor 2. dst....
17Cl35
· Lambang atom = Cl (Klor)
·
Massa atom = 35
·
Nomor atom = 17
·
Jumlah proton =
17
·
Jumlah elektron =
17
·
Jumlah neutron =
35-17 = 18
·
Konfigurasi
elektronnya adalah sebagai berikut:
K (2) L (8) M (7)
Dari konfigurasi elektron ini dapat diperoleh informasi bahwa atom Cl:
memiliki jumlah kulit 3 (ada di
periode 3).
memiliki elektron valensi 7
(berada pada golongan VIIA).
Elektron valensi adalah jumlah
elektron pada kulit terluar.
Agar stabil Cl cenderung
menangkap 1 buah elektron (menjadi Anion)
2.
Kation dan Anion
Secara alamiah atom dalam kondisi normal
memiliki jumlah proton dan elektron yang sama. Namun atom-atom yang jumlah
elektron pada kulit terluarnya tidak penuh atau tidak 8, maka atom tersebut
dalam keadaan tidak stabil. Atom-atom yang tidak stabil akan cenderung melepas
atau menangkap elektron. Atom yang melepas elektronnya, akan menjadi ion
positif (kation) sedangkan atom-atom yang menangkap elektron, akan menjadi ion negatif
(Anion).
3.
Ikatan Kimia
Ikatan kimia dibedakan menjadi ikatan ion dan
ikatan kovalen. Ikatan ion adalah ikatan antara ion positif dengan ion negatif.
Contohnya pembentukan natrium klorida (NaCl). Ikatan kovalen adalah ikatan
antar atom karena penggunaan elektron bersama. Contohnya adalah Cl2 dan
O2. Jika menggunakan sepasang elektron maka disebut ikatan konalen
rangkap satu, jika menggunakan dua pasang elektron maka disebut ikatan kovalen
rangkap dua, dan jika menggunakan tiga pasang elektron maka disebut eikatan
kovalen rangkap tiga.
D.
Sifat zat dan
hubungannya dengan partikel pemyusun dan strukturnya
1.
Sifat Fisika
Sifat fisika merupakan sifat yang dapat
diamati tanpa mengubah ciri-ciri dan komposisi suatu benda. Sifat fisika ini
juga dipengaruhi oleh atom dan ikatan antar atom yang menyusun benda. Contoh
sifat fisika antara lain: massa jenis (densitas), kekerasan, elastisitas, daya
hantar panas, daya hantar listrik, kemagnetan, viskositas (kekentalan), titik
didih, titik beku, dll.
2.
Sifat Kimia
Sifat kimia merupakan sifat yang tampak ketika benda tersebut mengalami perubahan secara kimia. Sifat kimia ini juga dipengaruhi oleh atom dan ikatan antar atom yang menyusun benda. Contoh sifat kimia antara lain: kestabilan, kereaktifan dan korosifitas.
Tugas 2 :
Jawablah
pertanyaan-pertanyaan berikut ini!
1.
Jelaskan
perbedaan antara kation dan anion!
2.
Apakah yang
dimaksud dengan ikatan ion? Sebutkanlah contohnya!
3.
Apa yang dimaksud
dengan ikatan kovalen? Sebutkanlah contohnya!
4.
Perhatikanlah
lambang atom berikut!
11Na23
a.
Lambang atom = …
b.
Massa atom = …
c.
Nomor atom = …
d.
Jumlah proton = …
e.
Jumlah elektron = …
f.
Jumlah neutron = …
g.
Konfigurasi
elektron = …
h.
Jumlah kulit = …
i.
Elektron valensi = …
j.
Kestabilan = …
k. Agar stabil cenderung = …
Kegiatan Belajar 3 :
Setelah kamu mengetahui sifat fisika dan sifat kimia suatu materi serta hubungannya dengan ikatan kimia yang terbentuk, berikutnya lakukanlah kegiatan berikut, untuk mengetahui serta memahami sifat kimia dan sifat fisika bahan dalam kehidupan sehari-hari.
Tugas 3
(Keterampilan):
Siapkanlah alat-alat
sebagai berikut!
·
Paku besi
·
Paku alumunium
(paku payung)
·
Asam cuka (jangan
terkena mata, jangan ditelan)
·
Lilin dan korek
api
·
Baterai, kabel
dan lampu
·
Palu
Lakukanlah sebuah
percobaan untuk menyelidiki sifat fisika dan kimia zat, kemudian bandingkanlah
antara sifat keduanya dan isikanlah hasilnya pada tabel berikut!
|
Sifat |
Paku besi |
Paku payung |
|
Kekerasan |
|
|
|
Elastisitas |
|
|
|
Daya hantar panas |
|
|
|
Daya hantar listrik |
|
|
|
Korosifitas |
|
|
Uji Kompetensi Bab Partikel Penyusun Benda dan Makhluk Hidup :
Jawablah dengan
cara memberi tanda silang pada huruf a, b, c atau d sebagai jawaban yang benar!
1. Perhatikan gambar umbi kentang
dan kayu berikut!
Manakah pernyataan berikut yang
salah?
a. Senyawa penyusun umbi kentang
dan kayu tersusun dari jenis atom yang sama
b. Senyawa penyusun umbi kentang
dan kayu memiliki jumlah atom yang sama
c. Umbi kentang dan kayu memiliki
sifat fisika dan kimia yang sama karena tersusun dari atom-atom yang sama
d. Umbi kentang dan kayu memiliki
sifat fisika dan kimia yang berbeda karena memiliki ikatan kimia yang berbeda
2. Seorang ilmuan yang memiliki
pendapat bahwa :
“Atom
sebagai bola yang di tengah tengahnya
terdapat inti atom yang merupakan pusat muatan positif dan pusat massa.
Sedangkan elektron-elektron berputar mengelilingi inti”.
a. Niels Bohr c.
J. John Thomson
3. Perhatikanlah gambar model atom
sebagai berikut!
Yang
merupakan Proton ditunjukkan oleh nomor ...
a. 1 c. 3
b. 2 d. 4
4. Perhatikanlah lambang atom
sebagai berikut ini!
11Na23
1) Massa atomnya adalah 23
2) Jumlah protonnya adalah 11
3) Jumlah elektron kulit
terluarnya adalah 11
4) Jumlah neutronnya 11
Pernyataan
yang benar berdasarkan lambang atom tersebut adalah ...
a. 1,
2 dan 3 c.
1, 3 dan 4
b. 1,
2 dan 4 d.
2, 3 dan 4
5. Atom-atom netral dapat berubah
menjadi ion. Berikut adalah pernyataan-pernyataan tentang terbentuknya ion.
1) Ion positif terbentuk karena
menangkap proton bebas
2) Ion negatif terbentuk karena
melepaskan protonnya
3) Atom yang melepaskan
elektronnya akan menjadi ion positif
4) Atom-atom yang menangkap
elektron bebas akan menjadi ion negatif
Pernyataan-pernyataan
yang benar adalah ...
a. 1 dan 2 c. 2 dan 3
b. 1 dan 3 d. 3 dan 4
6. Perhatikan pernyataan berikut!
1. Atom yang melepaskan sebuah
elektron
2. Atom yang menangkap dua buah
elektron
3. Atom yang jumlah elektronnya
lebih banyak dari jumlah protonnya
4. Atom yang jumlah protonnya sama
dengan jumlah elektronnya
Pernyataan yang sesuai dengan ion
negatif adalah ...
c. 1 dan 2 c. 2 dan 3
d. 1 dan 3 d. 3 dan 4
7. Perhatikan tabel berikut!
|
Bilangan
kuantum (n) ke |
Nama Kulit
Atom |
Daya Tampung
Elektron Maksimum |
|
1 |
K |
2 |
|
2 |
L |
8 |
|
3 |
M |
18 |
Berdasarkan
tabel tersebut, jumlah elektron maksimum yang dapat ditampung oleh kulit O
adalah ...
a. 28 c.
50
b. 32 d. 72
8. Di alam jarang sekali ditemukan
atom-atom dalam keadaan bebas melainkan dalam keadaan berikatan dengan atom
lain baik yang sejenis maupun tidak sejenis membentuk molekul dalam ikatan
kimia.
Berikut ini manakah yang
terbentuk melalui ikatan kovalen rangkap 2 ?
a. H dengan jumlah elektron 1 c. N dengan jumlah
elektron 7
b. O dengan jumlah elektron 8 d. Mg dengan jumlah elektron
12
9. Intan bersifat sangat kuat dan
keras serta memiliki titik lebur yang sangat tinggi. Hal ini disebabkan karena
intan memiliki ... .
a.
Ikatan
ion antar atom C yang sangat kuat
b.
ikatan kovalen antar atom C membentuk struktur tetra hedral
c.
elektron yang mudah bergerak dalam strukturnya
d.
proton
dan neutron yang sangat kuat
10. Berikut ini yang termasuk sifat fisika adalah ... .
a. viskositas, kekerasan, dan
elastisitas
b. kestabilan, korosifitas, dan
kereaktifan
c. viskositas, konduktivitas, dan
kestabilan
d. korosifitas, elastisitas, dan kemagnetan
Salinlah jawabanmu, kemudian pindahkan ke link berikut agar dapat dinilai!
https://forms.gle/NZWfKhW3EPftL5ZU6
C. RANGKUMAN
1. Setiap
benda dan makhluk hidup tersusun oleh molekulmolekul. Molekul ini tersusun atas
partikel yang lebih kecil yaitu atom.
2. Atom
tersusun atas partikel subatom yaitu proton yang memiliki muatan positif, elektron
yang memiliki muatan negatif, dan neutron yang tidak bermuatan.
3. Selain
disusun oleh molekul yang berbeda, sifat-sifat suatu materi atau benda yang berbeda
juga dapat disebabkan oleh perbedaan susunan molekul-molekul dalam materi itu.
4. Ada
beberapa teori perkembangan atom, yaitu teori Dalton, Thomson, Rutherford,
Bohr, dan teori atom modern.
5. Partikel
subatom, misalnya elektron banyak digunakan dalam berbagai bidang, misalnya
dalam mikrokskop elektron dan sinar-X.
6. Setiap atom
memiliki nomor atom dan nomor massa. Nomor atom menunjukkan jumlah proton,
sedangkan nomor massa menunjukkan penjumlahan proton dan neutron.
7. Molekul dan
atom yang menerima atau melepas elektron menjadi bermuatan dan membentuk ion.
8. Proses
pembentukan ion itu disebut ionisasi. Ion yang bermuatan positif disebut kation.
Sedangkan ion yang bermuatan negatif secara umum disebut anion. Gaya
tarik-menarik antara kation dan anion dalam senyawa tersebut disebut ikatan
ionik.
9. Pembentukan
ikatan kimia melalui penggunaan bersama elektron antardua atom disebut dengan
ikatan kovalen.
10. Susunan
elektron di dalam suatu atom disebut dengan konfigurasi elektron.
11. Tingkat
energi dalam suatu atom berturut-turut adalah tingkat energi K atau n=1 yang
dapat ditempati oleh 2 elektron, L untuk n=2 yang dapat ditempati oleh 8
elektron, M untuk n=3 yang dapat ditempati oleh 18 elektron dan seterusnya.
12. Uji nyala
dapat digunakan untuk mengetahui kandungan beberapa unsur dalam suatu senyawa
secara sederhana.
13. Intan dan
grafit tersusun dari atom yang sama yaitu atom karbon (C), namun membentuk
struktur dan jenis ikatan yang berbeda sehingga dapat dihasilkan karakteristik
yang berbeda. Pada intan masing-masing atom karbon (C) mengikat
empat atom karbon (C) lainnya dengan ikatan kovalen membentuk struktur tetrahedral.
14. Ada
beberapa jenis plastik didasarkan pada bahan penyusunnya, yaitu plastik PETE,
HDPE, PVC, LDPE, PP, PS, dan jenis lain.
15.
Masing-masing jenis plastik memiliki karakteristik yang berbeda sehigga
pemanfaatannya juga perlu memperhatikan karakteristik dari jenis plastik
tersebut.
16. Ada banyak
jenis logam yang bermanfaat dalam kehidupan sehari-hari, misalnya baja, stainless
steel, galvalum, perunggu,
dan kuningan. 17.
Suatu logam dapat dipadukan dengan logam yang lain sehingga
dapat
diperoleh sifat yang baru. 18. Tulang tersusun atas bagian yang hidup yaitu
sel-sel tulang (osteosit) dan bagian tak hidup. Zat organik penyusun tulang
antara lain yaitu kolagen, proteinpolisakarida, dan glikoaminoglikan. Zat
anorganik penyusun tulang yaitu senyawa hidroksiapetit.
D. KUNCI JAWABAN
Tugas 1:
1. Karena setiap benda dapat tersusun dari jenis atom yang berbeda, jumlah atom-atom yang berbeda, serta ikatan kimia antar atom yang berbeda-beda.
2. Atom terdiri dari inti atom dan kulit atom. Inti atom berada ditengah dan terdiri dari proton dan neutron. kulit atom terbentuk sebagai tempat lintasan elektron yang terus bergerak mengelilingi inti atom.
3. Persamaan = tersusun dari jenis atom yang sama yaitu C,H dan O serta jumlah yang sama
Perbedaan = jenis ikatan antar C,H, dan O
4. a. Na; b. 23; c. 11; d. 11; e. 11; f. 12
Tugas 2:
1. Kation merupakan atom bermuatan positif, disebabkan telah melepaskan beberapa elektronnya, sedangkan anion merupakan atom bermuatan negatif, disebabkan menangkap beberapa elektron dari atom lain.
2. Ikatan ion adalah ikatan yang terjadi antara ion positif dan ion negatif, contohnya pembentukan NaCl.
3. Ikatan kovalen adalah ikatan antara atom karena penggunaan pasangan elektron bersama. Contohnya Cl2, O2 dan N2.
4. a. Na; b. 23; c. 11; d. 11; e. 11; f. 12; g. K (2) L(8) M (1); h. 4; i. 1; j. tidak stabil; k. melepaskan 1 elektron
Tugas 3 :
|
Sifat |
Paku besi |
Paku payung |
|
Kekerasan |
Kurang keras |
Keras |
|
Elastisitas |
Elastis |
Kurang elastis |
|
Daya hantar panas |
Baik |
Baik |
|
Daya hantar listrik |
Baik |
Baik |
|
Korosifitas |
Lebih cepat berkarat |
Lambat berkarat |
Uji Kompetensi:
1. c; 2. b; 3. a; 4. a; 5. d; 6. c; 7. c; 8. b; 9. b; 10. a
E. PENILAIAN
Setelah kamu mempelajari bab ini, maka penilaian akan dilakukan sebagai berikut.
1. Penilaian kompetensi sikap : Dilakukan selama proses pembelajaran daring dibuktikan dengan daftar hadir, kedisiplinan mengerjakan tugas, umpan balik berupa komentar, pertanyaan dan diskusi, dan kelengkapan tugas.
2. Penilaian kompetensi pengetahuan: Dilakukan diakhir pertemuan berupa tes tertulis secara daring melalui google form. link dan token akan dishare kemudian (tunggu saja ya!)
3. Penilaian kompetensi keterampilan: Tugas keterampilan adalah Tugas 3










Para siswa sekalian, silahkan belajar mandiri ya. karena waktu kita sangat terbatas, sehingga jalan terbaiknya adalah segera menyelesaikan tugas dan belajar sesuai dengan target
BalasHapusmau mengingatkan saja
BalasHapusMTK itu tidak wajib,yang wajib itu shalat